Когда слышишь слово ""соль"", то первая ассоциация, конечно же, поваренная, без которой любое блюдо покажется невкусным. Но ведь это не единственное вещество, которое относится к классу химических веществ соли. Примеры, состав и химические свойства солей вы сможете найти в этой статье, а также научитесь правильно составлять название любой из них. Прежде чем продолжить, давайте договоримся, в этой статье мы рассмотрим только неорганические средние соли (полученные при реакции неорганических кислот с полным замещением водорода).
Определение и химический состав
Одно из определений соли звучит так:
- Это бинарное соединение (т. е. состоящее из двух частей), в состав которого входят ионы металлов и кислотный остаток. То есть это вещество, получившееся в результате реакции кислоты и гидроксида (оксида) любого металла.
Есть еще одно определение:
- Это соединение, представляющее собой продукт полного или частичного замещения ионов водорода кислоты ионами металла (подходит для средних, основных и кислых).
Оба определение правильные, но не отражают всю суть процесса получения соли.
Классификация солей
Рассматривая различных представителей класса солей, можно заметить, что они бывают:
- Кислородсодержащими (соли серной, азотной, кремниевой и других кислот, в состав кислотного остатка которых входит кислород и еще один неметалл).
- Бескислородными, т. е. соли, образованные при реакции кислоты, кислотный остаток которой не содержит кислород, — соляная, бромоводородная, сероводородная и другие.
По количеству замещенных водородов:
- Одноосновные: соляная, азотная, иодоводородная и другие. В состав кислоты входит один ион водорода.
- Двухосновные: два иона водорода замещены ионами металлов при образовании соли. Примеры: серная, сернистая, сероводородная и другие.
- Трехосновные: в составе кислоты три иона водорода замещены металлическими ионами: фосфорная.
Есть и другие типы классификаций по составу и свойствам, но мы не станем их разбирать, так как цель статьи немного другая.
Учимся называть правильно
У любого вещества есть название, которое понятно только жителям определенного региона, его еще называют тривиальным. Поваренная соль — пример разговорного названия, по международной номенклатуре оно будет называться уже по-другому. Но в разговоре абсолютно любой человек, знакомый с номенклатурой названий, без проблем поймет, что речь идет о веществе с химической формулой NaCl. Эта соль является производной от соляной кислоты, а соли ее называют хлоридами, то есть называется она хлорид натрия. Нужно просто выучить названия солей, приведенных ниже в таблице, а затем добавить название металла, образовавшего соль.
Но так просто составляется название, если у металла неизменная валентность. А теперь рассмотрим соль (пример с названием), у которой металл с переменной валентностью — FeCl3. Вещество называется хлорид железа трехвалентного. Именно такое название правильное!
|
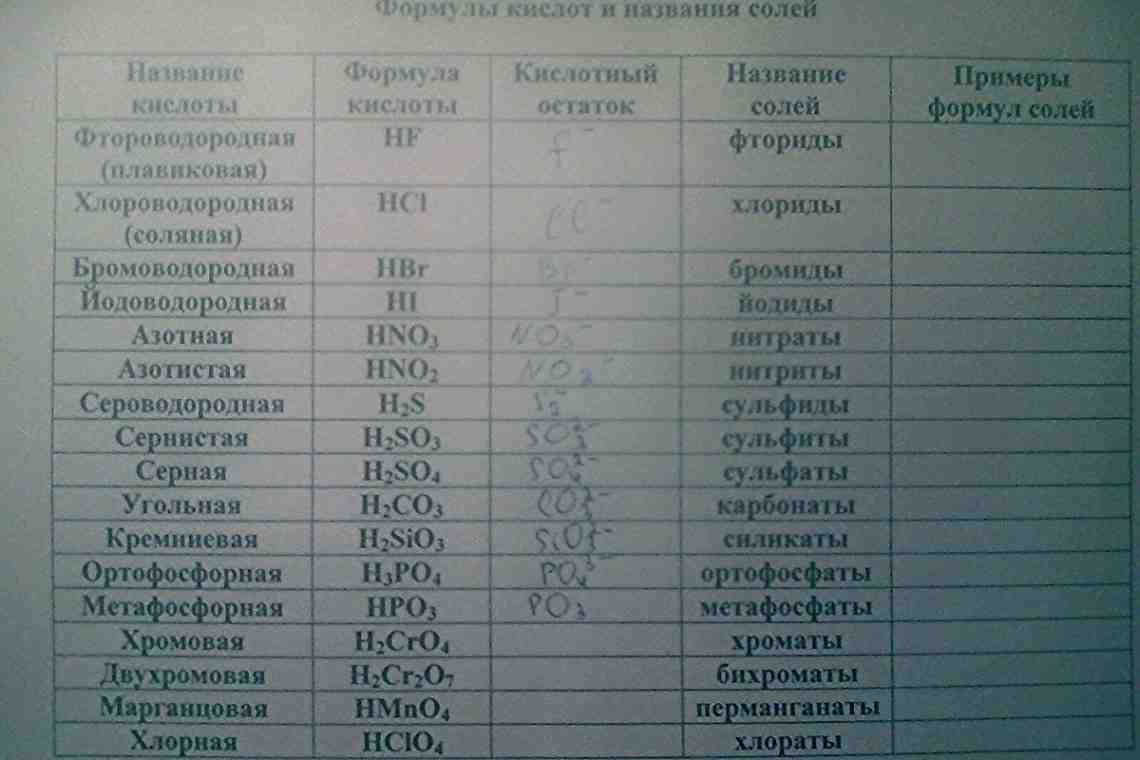
Формула кислоты |
Название кислоты |
Кислотный остаток (формула) |
Номенклатурное название |
Пример и тривиальное название |
|
HCl |
соляная |
Cl- |
хлорид |
NaCl (поваренная соль, каменная соль) |
|
HI |
иодоводородная |
I- |
иодид |
NaI |
|
HF |
фтороводородная |
F- |
фторид |
NaF |
|
HBr |
бромоводородная |
Br- |
бромид |
NaBr |
|
H2SO3 |
сернистая |
SO32- |
сульфит |
Na2SO3 |
|
H2SO4 |
серная |
SO42- |
сульфат |
CaSO4 (ангидрит) |
|
HClO |
хлорноватистая |
ClO- |
гипохлорит |
NaClO |
|
HClO2 |
хлористая |
ClO2- |
хлорит |
NaClO2 |
|
HClO3 |
хлорноватая |
ClO3- |
хлорат |
NaClO3 |
|
HClO4 |
хлорная |
ClO4- |
перхлорат |
NaClO4 |
|
H2CO3 |
угольная |
CO32- |
карбонат |
CaCO3 (известняк, мел, мрамор) |
|
HNO3 |
азотная |
NO3- |
нитрат |
AgNO3 (ляпис) |
|
HNO2 |
азотистая |
NO2- |
нитрит |
KNO2 |
|
H3PO4 |
фосфорная |
PO43- |
фосфат |
AlPO4 |
|
H2SiO3 |
кремниевая |
SiO32- |
силикат |
Na2SiO3 (жидкое стекло) |
|
HMnO4 |
марганцовая |
MnO4- |
перманганат |
KMnO4 (марганцовка) |
|
H2CrO4 |
хромовая |
CrO42- |
хромат |
CaCrO4 |
|
H2S |
сероводородная |
S- |
сульфид |
HgS (киноварь) |
Химические свойства
Как класс, соли по своим химическим свойствам характеризуются тем, что могут взаимодействовать со щелочами, кислотами, солями и более активными металлами:
1. При взаимодействии со щелочами в растворе обязательным условием реакции является выпадение в осадок одного из получаемых веществ.
2. При взаимодействии с кислотами реакция проходит, если образуется летучая кислота, нерастворимая кислота или нерастворимая соль. Примеры:
- К летучим кислотам относится угольная, так как она легко распадается на воду и углекислый газ: MgCO3 + 2HCl = MgCl2 + H2O + CO
- Нерастворимая кислота — кремниевая, образуется в результате реакции силиката с другой кислотой.
- Одним из признаков химической реакции является выпадение осадка. Какие соли выпадают в осадок, можно посмотреть в таблице растворимости.
3. Взаимодействие солей между собой происходит только в случае связывания ионов, т. е. одна из образовавшихся солей выпадает в осадок.
4. Чтобы определить, пойдет ли реакция между металлом и солью, нужно обратиться к таблице напряжения металлов (иногда ее еще называют рядом активности).
Только более активные металлы (расположенные левее) могут вытеснять из соли металл. Примером является реакция железного гвоздя с медным купоросом:
CuSO4 + Fe= Cu + FeSO4
Такие реакции свойственны большинству представителей класса солей. Но есть и более специфические реакции в химии, свойства соли индивидуальные отражающие, например разложение при накаливании или образование кристаллогидратов. Каждая соль индивидуальна и по-своему необычна.